
اقتراحات بور
1- ان لذرة الهيدروجين مستويات طاقة معينة يمسح للالكترونات ان تتواجد فيها
2- ان للالكترون في ذرة الهيدروجين يتحرك حول النواه في مدارات دائرية مسموح بها فقط
3- تخصيص لكل مدار عدد صحيح (n)
4- ان ذرة الهيدروجين تكون في الحالة المستقرة عندما يكون الالكترون الوحيد في مستوى الطاقة n=1
حالة الاستقرار: الحالة التي تكون فيها الكترونات الذرة ادنى طاقة
حالة اثارة : عندما تكتسب الذرة الكترونات
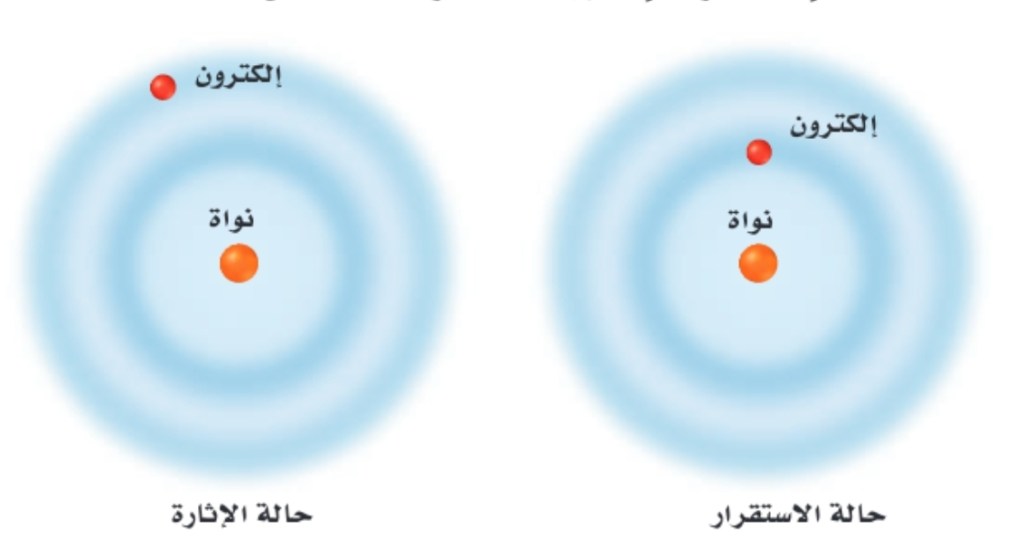
العدد الكمي : العدد الصحيح المخصص للمدارارت
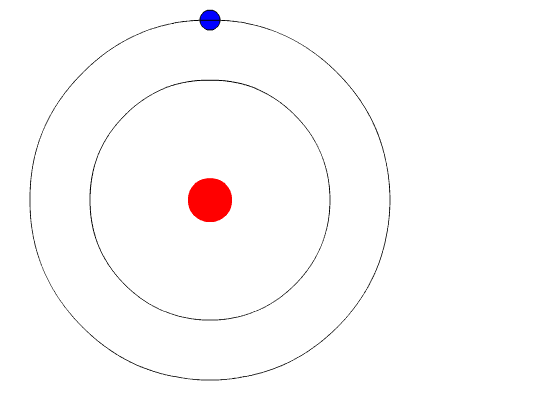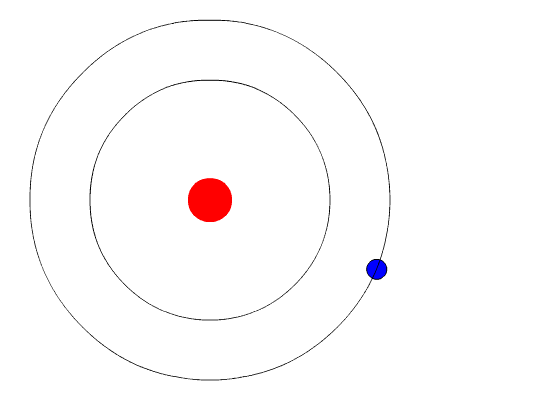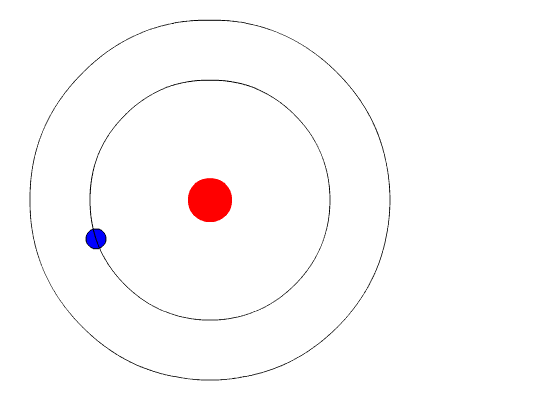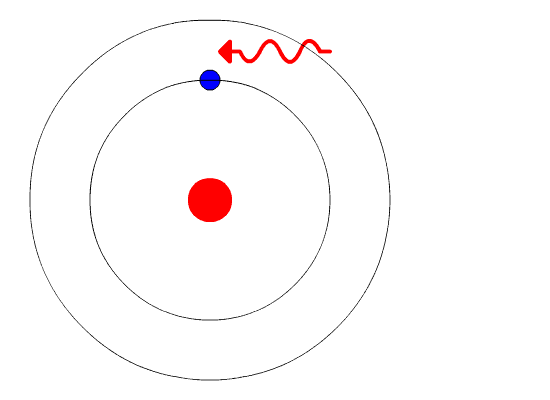
عند اضافة طاقة من مصدر خارجي الى الذرة يتنقل الالكترون الى مستوى طاقة اعلى و يجعل هذا الانتقال الذرة في حالة إثارة و يمكن ان ينتقل الالكترون من مستوى الطاقة الالعلى الى مستوى الطاقة الالق فترسل الذرة فوتونا طاقته تساوي الفرق بين طاقة المستويين
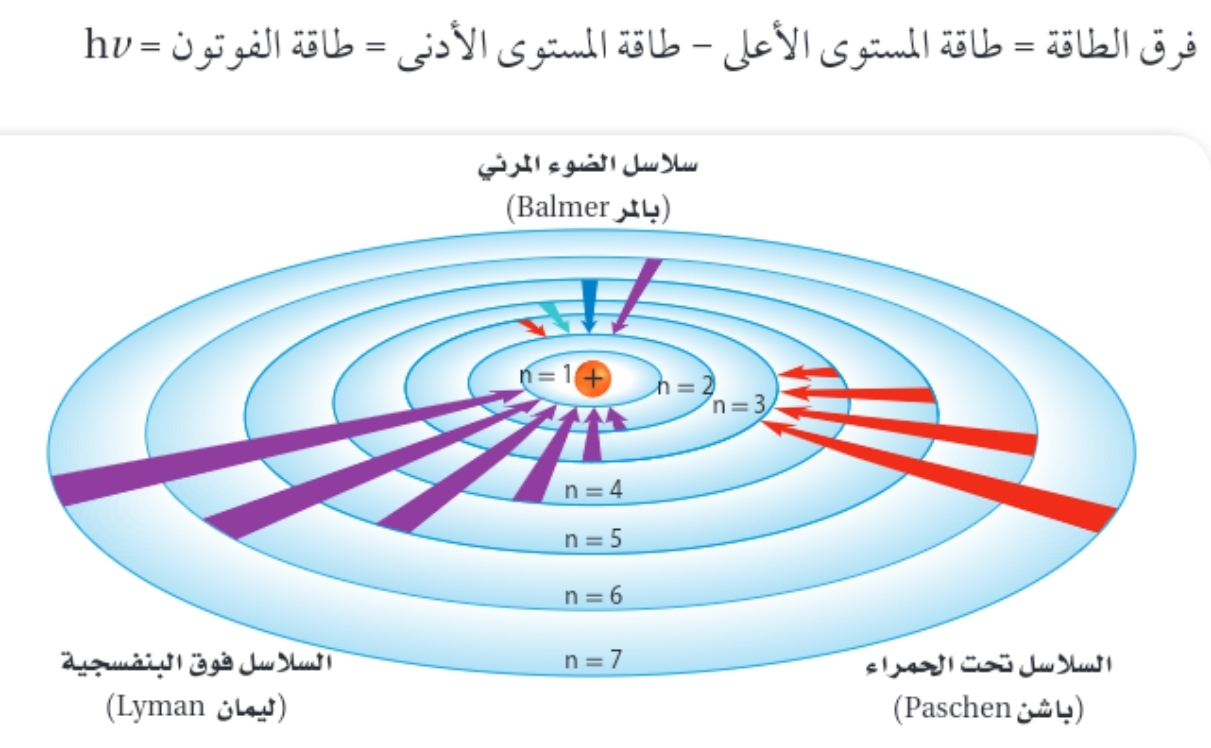
السلاسل ومستوى الطاقة التي ينتقل اليه الالكترونات :
ليمان > سلاسل فوق البنفسجية n=1
بالمر > المرئية n=2
باشن > تحت الحمراء n=3
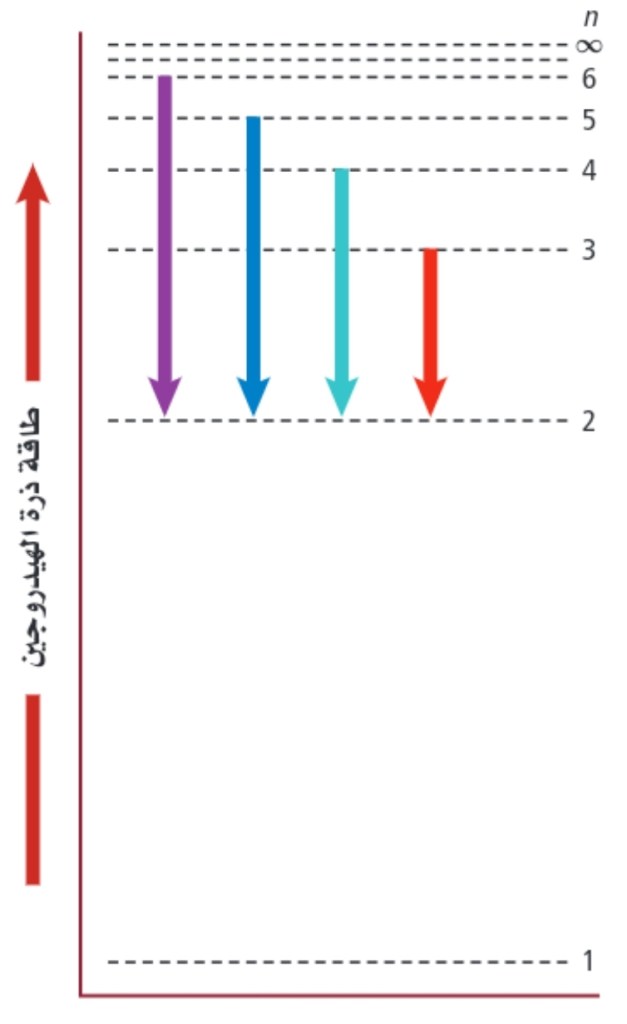
يمكن للالكترون الانتقال من مستوى مسموح به الى اخر فقط و لا يبعد مستويات الطاقة بعضها عن بعض مسافات متساوية
حدود نموذج بور :-
1- لم يفسر طيف اي عنصر غير الهيدروجين كما انه لم يفسر السلوك الكيميائي للذرة
2- هناك ادلة تؤكد ان الالكترونات لا تتحرك حول المواه في مدارات دائرية كما لو انها مسطحة